发布者:中国兽医协会发布时间:2026-01-14阅读次数:
各省、自治区、直辖市农业农村(农牧)、畜牧兽医厅(局、委),新疆生产建设兵团农业农村局,中国兽医药品监察所:
为规范兽药研究活动,根据《兽药管理条例》、《兽药非临床研究质量管理规范》、《兽药临床试验质量管理规范》以及监督检查办法和标准,我局组织专家对山东景佑医药科技有限公司、北京英太格瑞生物科技有限公司进行了监督检查。经监督检查,山东景佑医药科技有限公司等2家单位的15个试验项目符合兽药临床试验质量管理规范(以下简称“兽药GCP”)要求,现将监督检查结果予以公布(见附件)。
广东永顺生物制药股份有限公司等7家单位申请增加兽药GCP动物试验场所、青岛德济农科生物科技有限公司等2家单位申请变更兽药GCP动物试验场所名称、北京远大星火医药科技有限公司等2家单位申请变更兽药GCP项目负责人、天康生物制药有限公司等2家单位申请变更兽药GCP机构负责人,经我局组织资格确认,符合相关要求,详细信息见中国兽药信息网“兽药GLP/GCP监督检查”专栏。
请各省级畜牧兽医主管部门切实做好日常监督管理工作,督促相关单位按照规范要求开展兽药研究活动。
附件:符合兽药GCP要求的单位和试验项目
农业农村部畜牧兽医局
2026年1月9日
附件
符合兽药GCP要求的单位和试验项目
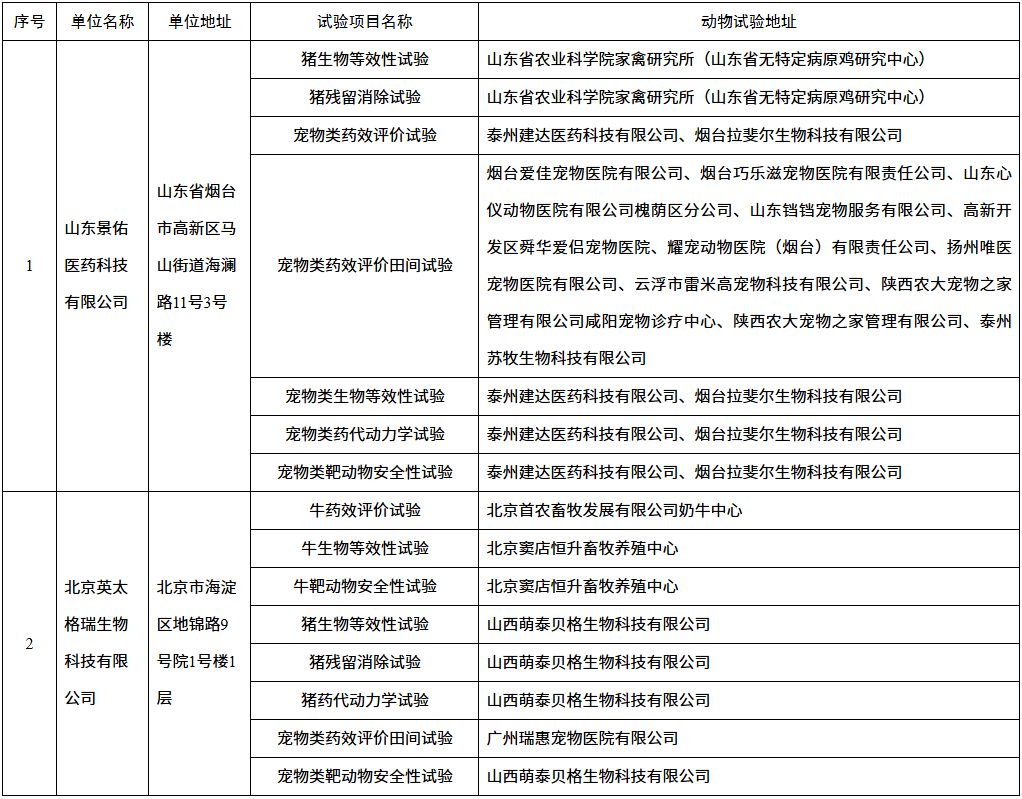
信息来源:农业农村部畜牧兽医局